Hensikt
Sikre at utførelsen av analysen Retikulocytter (Retic) i blod på Sysmex XN gir et korrekt og optimalt svar til rekvirenten.
Omfang
Prosedyren gjelder alle som har fått opplæring i analysering av Retic, og som har Sysmex som arbeidsoppgave.
Se ALM-; Opplæring, oppdatering og vedlikehold/heving av kompetanse .
Grunnlagsinformasjon
HISTORIKK
Levanger:
Retikulocytter ble analysert på CellDyn Sapphire (fra 30/5-2012) og Sysmex XN-1000 (fra høsten 2015). Tidligere har det blitt analysert på Sysmex XT 2000i, CellDyn 4000 og Coulter Max-M. Før den tid ble retikulocytter telt manuelt i Millers okular.
Namsos:
Retikulocytter har vært analysert maskinelt siden høsten 2001.
Før den tid ble retikulocytter kvantitert manuelt i mikroskop ved bruk av Millers okular.
Fra høsten 2001 til høsten 2003 ble CellDyn 4000 benyttet til å kvantitere retikulocytter.
Fra høsten 2003 til mai 2011 ble Sysmex XT 2000i benyttet til dette.
Siden 30. mai 2011 er retikulocytter kvantitert ved hjelp av CellDyn Sapphire.
Siden høsten 2015 blir retikulocytter også kvantitert på Sysmex XN-1000.
Fra 15/5-19 blir reticulocytter analysert på Sysmex XN-1000 og XN-1500 på begge sykehus.
ANALYSEPRINSIPP OG TERMINOLOGI
Terminologi 3)
Retikulocytter er unge erytrocytter som inneholder en del mitokondrier, noen ribosomer og et Golgi-apparat. Når slike celler supravitalfarges, får vi aggregasjon av ribosomer og mitokondrier. Aggregatene tar opp farge og i mikroskop ser dette ut som et småklumpet nettverk (retikulum). Retikulocytter tilbringer normalt to døgn i beinmargen før de slippes ut i sirkulasjonen. Etter ytterligere to døgn i sirkulasjon er det så lite organeller tilbake i cellene at de ikke lenger kan regnes som retikulocytter. Erytropoietin øker erytropoesen og stimulerer frigjøringen av retikulocytter fra beinmargen. Økt erytropoietinsekresjon ved akutt anemi forkorter retikulocyttenes modningstid i beinmargen og øker retikulocyttmengden i blod før produksjonen av erytrocytter reelt er økt. Analyse av retikulocytter ble tidligere utført med en manuell og relativt upresis metode. På de aller fleste laboratorier utføres nå denne celletellingen maskinelt. En slik retikulocyttbestemmelse gir langt mer presise resultater, særlig i lave områder. I tillegg gir maskinell metode mulighet for bestemmelse av retikulocyttfraksjoner, dvs. en gruppering av cellene med hensyn til modningsgrad. Flere hematologi-instrumenter utgir Immature Reticulocyte Fraction (IRF) som representerer den relative andel av de yngste retikulocyttene (de yngste blant de unge) og er et mål på de cellene som nylig er produsert i beinmargen. Dette gir mulighet for å oppdage selv små forandringer i den effektive erytropoiesen på et tidlig stadium.
Analyseprinsipp 2)
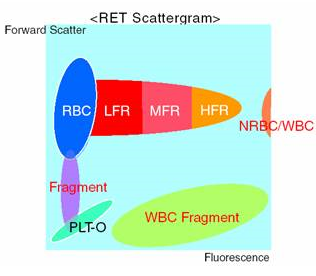
Til telling av retikulocytter benyttes RNA/DNA farging med polymethin. Innholdet av RNA- fragmenter detekteres ved hjelp av fluorescenssignal i flowcellen. Desto mer umodne retic i pasientprøven, jo lengre mot høyre i scattergrammet vil cellene være. Retikulocyttene deles opp i 3 ulike modenhetsfraksjoner ut fra modningsgrad; LFR, MFR og HFR (lav fluorescens-, middel fluorescens- og høy fluorescens retikulocytter).
Instrumentet benytter videre fraksjonene MFR og HFR til å beregne IRF (Immature Reticulocyte Fraction) eller umodenhetsfraksjon.
Prinsippene som
benyttes er cellenes størrelse (Foreward Scatter) og innholdet RNA (Side
fluorescens).
Dette er en helautomatisk metode. Det er ikke behov for manuell forfortynning.
Det er få
interferenser på denne metoden. Malariaplasmodier kan gi falsk for høye retikulocyttverdier.
De inneholder RNA og vil dermed kunne generere fluorescens signal. Ellers ingen
interferenser av betydning uten at instrumentet varsler.
Instrumentet gir ut retikulocytter i absolutt tall # og i %, samt i modenhetsfraksjoner (IRF).
IRF er de 2 mest umodne fraksjonene av retic: HFR og MFR.
IRF er en av de tidligste parameterne som øker ved økt erytropoietin-aktivitet, hvis benmargen fungerer slik den skal.
Medisinsk indikasjon 3)
Se
REFERANSER
Hovedreferanse:
(1) Sysmex brukermanual. Versjon 22 og sensere. Sist revidert aug 2022
Tilleggsreferanser:
(2) Generell produktinformasjon Sysmex. Mottatt 2018.
(3) Nasjonal brukerhåndbok i Medisinsk Biokjemi (J. Stakkestad, A. Åsberg m.fl.)
(4) Holdbarhetstabell for analyser ved Seksjon for hematologi AMB, SOH. EQSDocument 26842 v. 3.5
Offisielle godkjenninger:
(5) Leverandør oppgir å være ISO 9001 sertifisert. Utstyr og reagenser er CE-merket etter IVD direktivet.
Interne valideringer:
(6) Analysen har blitt kontrollert siden oppstart med daglige kvalitetskontroller og eksterne kvalitetskontroller og resultatene har vært tilfredsstillende. Se metodens ytelse.
(7) Valideringsrapport: ALM-MB-Hem; Validering av SYSMEX XN-1000 (Ikke tilgjengelig) og ALM-MB-Hem; Validering av Sysmex XN-1500 (Ikke tilgjengelig)
Høring:
Prosedyren har vært til høring hos overlege, fagbioingeniør og spesialbioingeniør.
METODENS YTELSE
Måleusikkerhet:
Det er beregnet gjennomsnittlig CV for instrumentet målt i kontrollblod i to nivå. Hver måned blir det vurdert mean, SD, CV og antall kontroller som er kjørt. Dataene lagres.
Måleområde/Linearitet:
Retic:
0,01-0,72 . 1012/L
Presisjon/Nøyaktighet:
Se valideringsrapport
Standarder/Kalibratorer
Sysmex XN kalibreres med Sysmex XN CAL, levert av Sysmex. Kalibreres etter service og ellers ved behov.
Verdiene på kalibratoren er hentet fra replikate kjøringer på referanseinstrument som er kalibrert i henhold til NCCLS og ICSH-anbefalt metode, referansemetode.
INTERN KVALITETSKONTROLL
Det benyttes to kommersielle kontroller og pasientprøver som interne kvalitetskontroller:
· Kommersielle kontroller, brukes hver dag i 2 nivå.
· Pasientprøver
o Samkjøring mellom instrumentene
o X-M – pasientmean over tid
EKSTERN KVALITETSKONTROLL
Vi benytter kontroller fra NOKLUS som ekstern kontroll, og følger deres program for kontrollnivå og hyppighet.
Resultatene
ligger i kvalitetssystemet EQS.
Henviser til ALM-; Sammenlignende laboratorieprøvinger (SLP, ekstern kvalitetskontroll, ringtest) - håndtering og vurdering
ANALYTISK KVALITET
Tillatt totalfeil (TEA): 30 % (Faglig vurdering)
Arbeidsbeskrivelse
Kort oversikt over Retikulocytter
· Prøvemateriale: EDTA-blod, CITRAT-blod.
· Prøvevolum: 88 µL i både auto og manuell mode.
· Standardpipettering: Ufortynnet.
· Metoder på instrumentet: Fluorescens flowcytometri og optisk måling
· Betegnelse på instrumentet: Ret
· Betegnelse i datasystemet: b-Retic
· Kalibratorer: Retic kalibreres Sysmex XN CAL
· Kontroller: XN Chek L, N og H og pasientprøver
· Reagenser: Cellpack DFL, Fluorcell Ret.
· Benevning: 1012/L
· Måleområde: 0,01-0,72 · 1012/L
ANSVAR
Fagbioingeniør
og / eller spesialbioingeniør har ansvar for prosedyren og oppdatering av
denne. Alle som har fått opplæring og er godkjent for analysering på Sysmex er
ansvarlig for at prosedyren blir fulgt. Se Omfang
HMS/sikkerhetsinformasjon
Alle blodprøver, kontroller og kalibratorer skal behandles som potensielt smittefarlig. Se prosedyre for Usterile engangshansker. Valg og bruk av usterile hansker.
HMS-datablad for reagensene forefinnes i Ecoonline.
ARBEIDETS GANG
Spesielle forhold vedr. prøvetaking og forberedelse av pasient
Henviser til ALM-MB-Hem; Sysmex XN, Erytrocytter (Epk) i fullblod
Prøvematerialet og bearbeidelse av dette
Henviser til ALM-MB-Hem; Sysmex XN, Erytrocytter (Epk) i fullblod
· Holdbarhet:4) Ved temperatur 2 til 25 °C:
o Retic: 72 timer.
Reagenser og klargjøring av disse
Leverandør: Sysmex Norge
Alle reagenser kommer klare til bruk, og oppbevares i romtemperatur.
· Cellpack DFL
Holdbarhet:
Uåpnet: Til utløpsdato
På instrumentet: 60 dager.
Volum: 1,5 L.
· Fluorcell Ret (Kreftfremkallende)
Holdbarhet:
Uåpnet: Til utløpsdato
På instrumentet: 90 dager.
Volum: 12 mL.
Avhending: Hullet på pakningen lukkes med tape før den kastes!
Analyseutstyr og klargjøring av disse
Sysmex
klargjøres etter prosedyre ALM-MB; Sysmex XN.
Feilkilder og interferens
· Falskt for høy:
o Kuldeagglutininer (pga at RBC blir falskt for lav)
o Malaria-plasmoider
o Howell Jolley bodies
o Store, RNA-rike trombocytter
o Fragmenterte leukocytter
· Falskt for lav:
o Hemolyse
Fremgangsmåte/Utførelse av analysen
Se prosedyre ALM-MB; Sysmex XN.
Beregning av svar
Svarene fra analyseinstrumentet gis direkte ut, men må korrigeres ved bruk av annet prøvemateriale enn EDTA.
· Ved bruk av CITRAT-glass multipliseres # Retic-resultatet med 1.11.
· Ved bruk av SR-glass multipliseres # Retic-resultatet med 1.25.
REFERANSEOMRÅDER
Ref. området
for voksne er funnet ved innkjøring av eget materiale (prøver fra 267
blodgivere) på Sysmex XN i 2015 ved SOH.
Barn: K.R. Herkner; A. Bøck, A. Muhl, S. Neubauer og C.Herkner; Pediatriske
referanseverdier for retik; Sysmex Journal International Vol.2 No.1 (1992)
Oppfølgende tiltak i forbindelse med svar
Se
ALM-MB; Sysmex XN Resultathåndtering i EPU
Vurdering og godkjenning av svar
Svarene autoverifiseres i EPU og overføres direkte til Beaker.
Svar som ifølge verifiseringsreglene ikke blir autoverifisert, vurderes manuelt (se under oppfølgende tiltak i forbindelse med svar) og godkjennes i Beaker.
Autoverifiseringen er satt til å gjelde svar > 0,01 og < 0,35 . 1012/L. Svar utenfor disse grensene og/eller alarm på en eller flere analyser i prøven, blir holdt tilbake for manuell vurdering.
Retic < 0,01 . 1012/L (under måleområdet) gis ut som < 0,01 . 1012/L.
Svarrapportering
Se
ALM-MB-IKT; Manuell overføring av prøvesvar fra analysemaskin til online-PC og
ALM-IKT; Svarrapportering, Beaker,
videre svarrapportering er etter Avdeling for laboratoriemedisin sine rutiner.