Arbeidsbeskrivelse
ANSVAR
Levanger: Fagbioingeniør ved faggruppen genteknologi har fagansvaret for instrumentet. Med. Mikrobiologi (MM) har ansvar for vedlikehold av instrument og hovedansvar for analysering av prøvene i deres åpningstid. Medisinsk Biokjemi analyserer prøver utenom åpningstiden til MM.
Namsos: Fagbioingeniør preanalytisk har fagansvaret for instrumentet. Medisinsk Biokjemi har ansvar for vedlikehold av instrument og analysering av prøvene i henhold til egne rutiner.
Levanger og Namsos: Alle ansatte som er opplært og utfører analysen har ansvar for å følge prosedyren.
HMS/sikkerhetsinformasjon
Siden humant materiale benyttes vil det alltid være en risiko for infeksjon. For å unngå kontaminering og infeksjon bør man alltid følge en standard sikkerhetsprosedyre ved håndtering av potensielt infeksiøst materiale: Se ALM-MM-; Hygiene og sikkerhetsrutiner på Lab. for med. mikrobiologi
· Alt arbeid med prøvene skal foregå i sikkerhetsskap klasse 2.
· Bruk smittefrakk og hansker ved alt arbeid med prøvene.
· Ved oppsett av flere prøver, skift hansker mellom hver prøve.
· Når prøven er tilsatt kassetten, knyt igjen søppelpose og kast den i risikoavfall.
· Bruk hansker til vaskeprosessen.
ARBEIDETS GANG
Prøvemateriale
Tabell 1: Oversikt over godkjent prøvemateriale
|
Prøvelokalisasjon |
Kan benyttes |
|
Prøve tatt fra nasofarynks og hals, tatt med samme tynne vattpinne i ett rør. |
JA |
|
Prøve tatt fra nasofarynks, tatt med tynn vattpinne. |
JA |
|
Prøve tatt fra både fremre nese (begge nesebor) og hals, tatt med samme Copan e-swab i ett rør. |
JA Resultatet må kommenteres: Mottatt prøvemateriale som ikke er validert av produsenten |
|
Prøve fra fremre nese |
JA Resultatet må kommenteres: Mottatt prøvemateriale som ikke er validert av produsenten |
|
Prøve tatt fra kun hals |
JA Resultatet må kommenteres: Mottatt prøvemateriale som ikke er validert av produsenten |
|
Ekspektorat mottatt på virus transportmedium (rød kork), Copan universal transportmedium (hvit, blå eller oransje kork) |
JA Resultatet må kommenteres: Mottatt prøvemateriale som ikke er validert av produsenten |
|
Ekspektorat eller BAL mottatt på universalcontainer. |
NEI Prøven må rekvireres til SOH |
Tabell 2: Oversikt over aktuelle prøvemedium
|
Godkjent fra leverandør |
Virus transportmedium (VTM) (Rød kork) Copan universal transportmedium (UTM) (Rød kork) |
|
Ikke validert, men kan benyttes |
Copan e-swab (blå, hvit eller oransje kork) Resultatet må kommenteres: Mottatt på prøvemedium som ikke er validert for denne metoden. |
Reagenser og klargjøring av disse
Reagenskit;
· Skal stå i romtemperatur. Har kassetten vært nedkjølt, skal testen utføres etter at kassetten er stabilisert i 30 minutter ved romtemperatur. Reagenskit-eskene står i hylle over M10.
· Rekvirering
Dette er i utgangspunktet en test som er tiltenkt inneliggende pasienter, men den kan også benyttes til pasienter fra sykehusets poliklinikker.
Prøvene skal komme ferdigrekvirert i Helseplattformen, men er prøven bestilt feil, må man endre analyse i Helseplattformen:
- Velg Prøveoppdatering
- Kontroller at det er valgt riktig beholdertype.
- Trykk Nye forordninger
- Velg X–Luftveisvirus, hurtigtest og trykk Godta
- Fyll inn prøvemateriale, prøvelokasjon og kliniske opplysninger (kopieres fra opprinnelig bestilling)
- Signer med autoriserende kliniker
- Avbryt analyser som er bestilt feil med avbrytelsesårsak «Feil analyse er rekvirert»
- Trykk Godta
Prøver mottatt fra Akuttmottak hvor det ønskes analysert RSV; Rekvirent må selv bestille ny «X- Luftveisvirus, hurtigtest» for å få svar på analysen. NB! Alle parameter skal svares ut til rekvirent.
Om prøver skal analyseres fra rekvirenter utenfor Helseplattformen rekvireres prøven i Beaker: Se ALM-MM-Mottak; Mottak, innregistrering og utsåing (Ikke tilgjengelig)
Vircell; AmpliRun® total SARS-CoV-2/Flu A/Flu B/ RSV Control (swab) (3)
· Skal oppbevares i kjøleskap.
· Glasset med det frysetørkede stoffet må ha romtemperatur før det løses opp med 500 µl sterilt vann/PCR-vann (gjerne UV-bestrålt). Bland til alt tørrstoffet er løst opp og vortex deretter i 30 sekunder slik at det blir en homogenisert løsning. Prøven blir deretter behandlet som en vanlig prøve.
· Det er ønskelig at KU-kontroll blir kjørt ved lot-skifte.
· Rekvirering:
- Rekvisisjonsoppføring
- Rekvirent:
For Levanger: HNT, Levanger SH., Avdeling for laboratoriemedisin, Medisinsk mikrobiologi {Ikkebet}{ikkeHP}{1235000009}
For Namsos: HNT, Sh. Namsos, Avdeling for laboratoriemedisin, Medisinsk biokjemi
- Pasient:
For Levanger:
Velg VIRCELL SARS-COV-2/FLUA/FLUB/RSV CONTROL og Godta
For Namsos: Velg VIRCELL SARS-COV-2/FLUA/FLUB/RSV/NAMSOS og Godta
- Prosedyre: X-Luftveisvirus, hurtigtest
- Opprett prøver
- Legg inn Prøvetakingsdato og Tidspunkt tatt
-
Rekvisisjonskommentar:
.RQI samt lot. Nr. til AmpliRun total-kittet og reagenslot for reagenskit som
brukes.
- Trykk Motta, godta og ny.
SLP;
· Rekvirering: Se ALM-MM; ALM-MM; SLP-kontroller mikrobiologi
Feilkilder og interferens
Utdrag fra produsentens pakningsvedlegg. For utfyllende informasjon om begrensninger se pakningsvedlegg under «Relatert».
Falske negative resultater kan forekomme av flere ulike årsaker. (1)
· Konsentrasjonen i prøven er nær eller under påvisningsgrensen for testen.
· Prøver blir innhentet, transportert eller håndtert på feil måte.
· Det er ikke tilstrekkelig mengde i luftveisorganismer til stede i prøven.
· Kassetter er eksponert for uheldige omgivelsesfaktorer (temperatur/luftfuktighet)
Fremgangsmåte/Utførelse av analysen
Oppbevaring av prøver før analysering
For prøver tatt på Virus/Universal transportmedium (rød kork) og Copan e-swab:
Tabell 3: Oversikt over prøvens holdbarhet
|
Romtemperatur 15-30°C |
Kjøleskap 2-8°C |
|
1 døgn (1) |
4 dager (1) |
Preparering av prøve og kassett (1)
Prøvene skal være romtempererte før analysering.
Preparering av prøvene skal gjøres i godkjent avtrekkskap (klasse 2). Bruk smittefrakk og hansker. Analyseres flere prøver så skal det skiftes hansker mellom hver prøve.
1. Prøven registreres i «mottak»
2. Fest liten etikett med instrument- og prøvenummer på kassettens framside.
3. Fjern sikkerhetsklemmen (blå) som er plassert under lokket på kassetten.
4. Press toppen av kassetten nedover for å punktere forseglingen ved bruk av puncheren.
5. Åpne lokket og sjekk at forseglingen er helt punktert før prøven tilsettes.
6. Bland prøven ved å vende prøverøret 5 ganger.
7. Overfør 300 µl av prøven i hullet på kassetten ved hjelp av eppendorf-pipette. Hullet er markert med en pil. NB! Prøvematerialet må tilsettes innen 10 minutter etter gjennomboring av kassetten.
8. Lukk lokket på prøvekassetten. NB! Så snart prøven har blitt tilsatt kassetten, må testen startes så snart som mulig (innen 30 minutter)
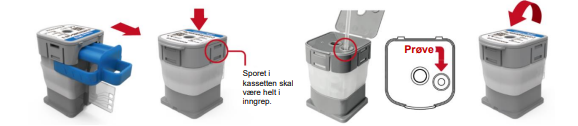
Figur 1: Preparering av kassett
Kjøring av STANDARD M10 influensa/RSV/SARS-CoV-2

Figur 2: M10 konsoll og modul
1. Om M10-konsollen står i dvalemodus, angi brukernavn og passord i påloggingsskjermbildet, og trykk Log In. Brukernavn og passord er angitt på konsollen.
2. Trykk på en ledig STANDARD M10-modul i skjermbildet Home for å kjøre. (døren til den valgte modulen vil åpnes automatisk for innsetting av kassett.)
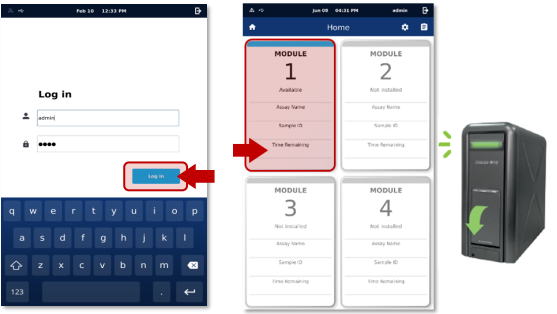
Figur 3: Skjermbilde hvor man velger modul
3. Angi prøve-ID ved å lese av strekkoden for prøven.
4. Les av kassetten som skal brukes. Instrumentet gjenkjenner automatisk analysen som skal kjøres.

Figur 4: Eksempel på hvordan man registrerer kassett og prøve på M10
5. Det vil så komme opp et skjermbilde som forklarer hvordan man preparerer prøven og kassetten for kjøring. Er dette steget gjort – gå videre til neste skjermbilde.
6. Neste skjermbilde angir hvordan kassetten skal settes inn i modulen. Gjør som angitt, og lukk døren helt. (OBS! vær forsiktig ved lukking av luke)
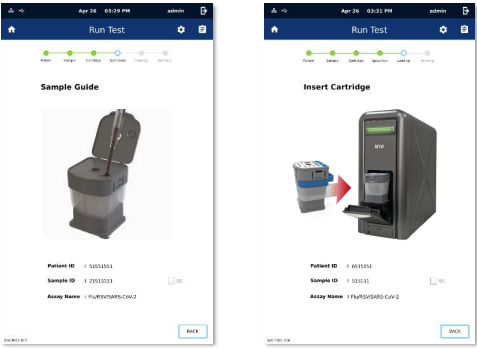
Figur 5: Skjermbilde før innsetting av kassett
7. Etter å ha bekreftet informasjonen om prøve og kassett, trykker man på OK-knappen på skjermen.
8. Analysen starter automatisk, og gjenværende tid vises på skjermen.
Testen tar 60 minutter, men instrumentet har en funksjon som heter «Early detection call» som gjør det mulig å se om prøven er positiv før det er gått 60 minutter. Avhengig av ct-verdi, vil det kunne komme opp resultat på positiv prøve (uten kurve) fra det er 30 minutter igjen av analysen.
Vurdering
Oppfølgende tiltak i forbindelse med svar
Early detection
Om funn av aktuelt agens gjøres, kan positivt svar foreligge så tidlig som 30 minutter med funksjonen «Early detection». Svaret vil ikke automatisk gå over til Beaker før analysen er ferdigkjørt.
Får man telefon med spørsmål om svar kan man bruke et evt. positivt svar fra «Early detection».
Analyseoppsett som feiler
Dersom analyseoppsett feiler retestes prøven med ny testkassett. Om retesting feiler – gi rekvirenten beskjed om at det må tas ny prøve. Prøven besvares Inkonklusiv og med kommentaren .NYPA (Ny prøve anbefales)
Etter analysering
1. Luken til modulen åpnes automatisk når prøven er ferdig analysert. Bruk hansker når kassetten plukkes ut. Kassetten kastes i en pose og kastes i risikoavfall.
2. Finn riktig prøvenummer i listen på skjermen (nyeste kjøring ligger øverst) og trykk på prøvenummeret. Resultatet vil da komme opp.
3. Trykk på «Amplification»-fanen for å kontrollere at kurvene har eksponentiell vekst. Sjekk alle tre kurvene på internkontrollene (IC) og kurven for aktuelt agens prøven er positiv på. Kurvene sjekkes kun på positive prøver.
Ved avvikende kurver på svar som allerede er autoverifisert, kontakt rekvirent og informer om usikkert svar. Be om en ny prøve.
Levanger: Prøveplassen har ansvar for å sjekke kurver
etter ferdig analysert prøve. Prøver kjørt på vakt sjekkes påfølgende morgen av
Medisinsk mikrobiologi.
Namsos: Den som analyserer prøven har ansvar for å sjekke kurven på
positive prøver. Unntak: Analyseres prøven på natt skal skillerom ha ansvaret
for å sjekke kurven påfølgende morgen.
For eksempel på kurver; se relatert.
Manuell svaroverføring fra M10 til Beaker
1. Finn riktig prøvenummer i listen på skjermen og trykk på prøvenummeret. Resultatet vil da komme opp.
2. Trykk på knappen «Send HL7» nederst til venstre side av skjermen. Prøvesvar skal da gå over til Beaker.
Svarrapportering
Negative resultater: Overføres automatisk til Beaker og autoverifiseres. Det er ikke nødvendig å ringe rekvirent.
Positive prøver:
Overføres automatisk til Beaker og autoverifiseres.
Unntak:
· Hvis IC er invalid for en av agensene vil prøven holdes tilbake i Beaker. Er prøven positiv for aktuelt agens er dette et godkjent svar, og prøven besvares som vanlig. Et høyt antall kopier av et målspesifikt gen kan føre til redusert eller fraværende IC. (1)
Prøver med ct > 36 vil automatisk få med kommentar .LAVI (lav virusmengde)
Positive resultat skal ringes ut til rekvirent.
· Velg Oppfølgingsliste og Visninger
· Trykk på Ringeoppgaver
· Finn aktuell prøve og skriv inn info om hvilken avdeling som er ringt, og hvem beskjeden er gitt til.
· Trykk Legg til hendelse, og Fullfør
NB! Husk å registrere i Komm. logg hvilken avdeling som er ringt, og hvem beskjeden er gitt til.
Tabell 4: Svarrapportering
|
Resultat |
Svarkode |
Automatisk analysekommentar |
Ringe svar? |
|
POSITIV Ct-verdi ≤ 37 |
POS |
Gjelder SARS-CoV-2: Analysen er gjort ved hjelp av nukleinsyreamplifikasjon/RT-PCR-metode The analysis was performed using nucleic acid amplification/RT-PCR technique MSIS-UM: MSIS-melding – klinikermelding skal ikke sendes. |
JA |
|
NEGATIV
|
NEG |
Gjelder SARS-CoV-2: Analysen er gjort ved hjelp av nukleinsyreamplifikasjon/RT-PCR-metode The analysis was performed using nucleic acid amplification/RT-PCR technique |
NEI |
Om rekvirent ønsker Ct-verdi på positivt agens;
- Gå inn i Resultatregistrering på aktuell prøve for å redigere resultat.
- Finn aktuelt agens rekvirent vil ha Ct-verdi på
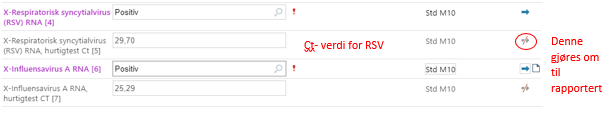
- Klikk på den grå pila til høyre for Ct-verdien (se Figur 6), og gjør denne om til «Rapportert»
- Verifiser prøven
Figur 6: Eksempel på rapportering av Ct-verdi for RSV
Vedlikehold
Daglig vedlikehold
· Tørk over arbeidsbenken med overflate desinfeksjonssprit.
· Sjekk touchscreen, barkodescanner og at døra åpnes (ved kjøring av prøve)
· Kast brukte prøvekassetter i en pose som knytes og kastes i risikoavfall.
Ukentlig vedlikehold
· Restart instrumentet. Slå av modulene først, og deretter konsollen. Slå deretter på igjen i motsatt rekkefølge. Når modulene lyser blått er instrumentet klart til bruk. (For pålogging: se opphengt påloggingsinformasjon på M10-konsoll)
Månedlig vedlikehold
· Desinfiser overflater på konsoll og moduler med 70% overflatedesinfeksjon.
· Vask kamrene i modulene.
- Åpne den skjulte menyen ved å tappe 8-10 ganger på «Home». Det vil komme opp en meny (se figur 7). OBS! Denne menyen kan ikke hentes fram når det står prøver å går på instrumentet.
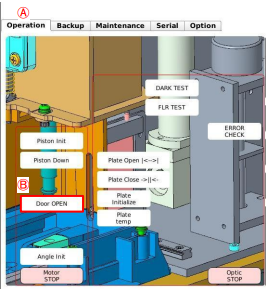
Figur 7: Bilde av skjult meny
- Velg deretter modul 1, 2 eller 3 til høyre i bildet og trykk «door open».
- Tørk forsiktig inni kammeret med en alkotip på anviste områder (se figur 8)

Figur 8: Områder markert skal vaskes med alkotip
- Trykk så «Piston down» i samme meny. Piston rod kommer ned.

- Tørk av piston rod med alkotip.
- Trykk deretter «Piston init» og lukk døren.
· Gjør Back-up av siste måneds kjøringer (Fag-/spesialbioingeniør/personell med spesiell opplæring)
- Sett en USB-pinne inn i USB-port på venstre side av konsollen.
- Gå til innstillinger og trykk «Register» under «USB Registration»
- Gå deretter til resultatlisten, og marker aktuelle prøver.
- Trykk på knappen «USB» nederst til venstre på siden.
- Når informasjonen er overført til USB-pinnen, skal det komme opp en melding om at overføringen er grei.
Ved behov (Fag-/spesialbioingeniør)
· Rengjør viftefiltrene og luftfiltrene.