Hensikt
Sikrer at identifisering av mikroorganismer utført på MALDI-TOF Sirius One blir utført på en korrekt måte.
Omfang
Alle bioingeniører som er opplært til å utføre denne type analysearbeid ved MM.
Snarveier
Grunnlagsinformasjon
Analyseprinsipp Og Terminologi
MALDI-TOF (matrix-assisted laser desorption/ionization- time of flight) er et massespektrometer.
En laser i instrumentet skyter mot en prøve krystallisert med matrix. Laseren vil spalte ribosomale proteiner i bakteriecellene til positivt ladede proteiner og peptider. Et elektrostatisk felt akselererer ionene, som vil vandre med forskjellig hastighet og nå detektoren på forskjellig tid. Instrumentet måler denne farten, som korrelerer til molekylær masse, og omgjør dette til et massespekter. Dette vil fungere som et molekylært fingeravtrykk som sammenlignes mot en referansedatabase med kjente mikrobers spektre.
Sepsityper kit inneholder reagens for å fjerne humane blodceller.
Referanser
1. MBT Compass HT IVD User Manual, Rev. E (March 2023)
2. MBT Compass Filamentous Fungi IVD Module User Manual, Rev.C (March 2023)
3. MBT HT Sepsityper IVD Module User Manual, Rev.C (October 2022)
4. Bruksanvisning IVD Bacterial Test Standard, Rev. L (Februar 2022)
5. Sammendrag 11 fra strategisamling 2024, ID av bakterier og sopp: IDENTIFIKASJON AV GJÆRSOPP MED MALDI-TOF MS
6. Sammendrag 13 fra strategisamling 2024, ID av bakterier og sopp: IDENTIFIKASJON AV ANAEROBER MED
MASSESPEKTROMETRI
7. Sammendrag 10 fra strategisamling 2024, ID av bakterier og sopp: IDENTIFIKASJON AV DERMATOFYTTER MED MALDI-TOF
8. Sammendrag 10 fra strategisamling 2024, ID av bakterier og sopp: IDENTIFIKASJON AV MUGGSOPP MED MALDI-TOF MS
9. Sammendrag 7 fra strategisamling 2024, ID av bakterier og sopp: IDENTIFIKASJON AV AEROBER OG FAKULTATIVT ANAEROBER – PRESISJON AV IDENTIFIKASJON, BEHOV FOR SUPPLERENDE FENOTYPISK TESTING OG RAPPORTERING AV SVAR
10. Sammendrag 3 fra strategisamling 2024, ID av bakterier og sopp: KVALITETSSIKRING OG HARMONISERING AV SVAR- RAPPORTERING AV BAKTERIE- OG SOPP ID VED MALDI-TOF MS
11. Sammendrag 3 fra strategisamling 2024, ID av bakterier og sopp: BIO-/LABSIKKERHET VED IDENTIFIKASJONSARBEID PÅ LAB – MALDITOF
Standarder/Kalibratorer
· IVD Bacterial Test Standard (BTS)
Intern Kvalitetskontroll
· IVD Bacterial Test Standard (BTS)
VD BTS inneholder et ekstrakt av Escherichia coli DH5-alfa, som viser en karakteristisk peptid- og proteinprofil i MALDI-TOF-massespektra. Ekstraktet er tilsatt to ekstra proteiner som utvider den øvre grensen for masseområdet dekket av IVD BTS. Generelt masseområde dekket av IVD BTS er m/z 3 600 til m/z 17 000.
Ekstern Kvalitetskontroll
· Ringtestprogrammet til FHI
· Neqas «General Bacteriology»
· Neqas «Mycology culture»
Arbeidsbeskrivelse
Ansvar
Fagbioingeniør for bakteriologi (gruppe 1) har ansvar for vedlikehold av prosedyren. Fagbioingeniør og spesialbioingeniør på faggruppen har ansvar for oppfølging etter service og vedlikehold. Superbrukere har ansvar for feilsøking og kontakt med servicetekniker. Opplærte bioingeniører har ansvar for daglig bruk og vedlikehold.
HMS/sikkerhetsinformasjon
· Engangsplater og Fast-shuttle benyttes til prøver i sikkerhetskabinett klasse 2 ved fæcesplass. Alt arbeid her utføres med nitrilhansker og frakk, og gjelder følgende arbeidsprosesser:
o Pellet fra blodkulturisolat.
o Isolat fra fæcesdyrkning. Skal alltid tilsettes maursyre.
o Prøvepreparering av muggsopp og dermatofytter utføres i sikkerhetskabinett klasse 2 for å unngå spredning av soppsporer i laboratoriet.
o Rutineisolat hvor man mistenker smitterisikogruppe 2 eller 3. Skal alltid tilsettes maursyre.
o Rutineisolat som testes med maursyre (eDT) eller ekstraksjon (EXT).
· Benytt hovedsakelig flerbruksplater til rutineisolat på benk. Alt arbeid på benk skal utføres med DT-metoden. Det er ikke nødvendig med beskyttelsesutstyr.
· Fortynnet maursyre skal tillages i eppendorfrør med skrukork (kryorør) for å unngå fare for sprut.
· Bruk syrehansker og sikkerhetskabinett på alt arbeid med ufortynnede kjemikalier. Ved håndtering av TFA skal ansiktet være beskyttet for eventuell sprut.
· MALDI-TOF skal IKKE gjøres ved mistanke om sporedannende bakterier som krever BSL3, det vil si ikke-hemolytisk Bacillus (Bacillus anthracis).
· Alle reagenser som brukes ved analyseringen kan være helseskadelige. Unngå søl på hud og i øynene.
Arbeidets Gang
Prøvematerialet og bearbeidelse av dette
Enkeltliggende isolat fra bakterier og sopp. Isolat inkubert i 1 døgn er å foretrekke. Se også dyrkningsforhold under feilkilder.
For sepsityper benyttes prøvemateriale fra positiv blodkulturflaske. 1 ml. tilsettes eppendorfrør i avtrekk på prøveplass før videre arbeid i avtrekk ved fæcesplass.
Reagenser og klargjøring av disse
OBS! Husk at alle kommersielle reagens som benyttes på Sirius skal være merket IVD.
Reagens benyttet til ekstraksjon, platevask og tillaging av OS overførøes/fortynnes og oppbevares i egne 50 ml-flasker på fargebenk. Disse byttes ut hver 3. mnd. Selve flaskene står i reagensskap under fargebenk. Alt arbeid med overføring/fortynning av syrer utføres i fæcesavtrekk med syrehansker og frakk.
· Sepsityper kit oppbevares i romtemperatur (15-25 °C) på pusslab (P062). Reagens er holdbare i opptil 3 måneder etter åpning.
· OS (Organic Solvent): Nylaget løsning benyttes til oppløsing av Matrix og BTS. Nylaget løsning kastes etter bruk.
Tillaging av OS:
1. Pipetter 475 µL HPLC-gradert vann i et eppendorf-rør.
2. Tilsett 25 µL 100% TFA (trifluoroacetic acid)
3. Tilsett 500 µL 100% ACN (acetonitril)
4. Vortex godt
· BTS: Kontroll og kalibrator til Maldi-TOF. Inneholder E.coli DH5 alpha spiket med to ekstra spekter som dekker opp øvre måleområde for masse. Uløst BTS oppbevares i fryser RTB062.1 på pusslab (P062).
1. Ta opp et BTS-rør fra fryseren (gul topp). La stå 5 minutter i romtemperatur før neste trinn. Dersom nytt LOT må dette registreres inn på instrument-PC. Gi beskjed til superbruker.
2. Bruk ny OS (OS=Standard Solvent). Pipetter 50 µL OS.
3. Bland med pipetten opp/ned minst 20 ganger. NB! Unngå luftbobler.
4. Inkuber i minst 5 min ved romtemperatur.
5. Repeter punkt 3.
6. Sentrifuger en kort stund, ca. 10 sekunder ved full hastighet.
7. Fordel 8 µL i Sarstedt mikrorør.
8. Frys ned ved minst -18 ºC, i fryseskap på pusslab. Benytt blå bokser. Påfør LOT og oppløst dato på lokk. Frossen IVD BTS-løsning kan lagres i opptil 5 måneder ved -18 °C eller lavere.
9. Signer på vedlikeholdsskjema i teams.
Preparering på plate
1. Romtemperer to rør fra fryseren i minst 5 minutter. Bland opp lett ved å knipse mot røret.
2. Sentrifuger ved full hastighet i ca. 10 sekunder. Plasser ett rør i avtrekk og ett rør på benk.
3. Pipetter 1 µL på spot. Tilsett 1 µL matrix når BTS er tørket.
OBS! Ved tilsetning av BTS på plate må matrix tilsettes innen 30 minutter etter at den har tørket. Etter tilsetning av matrix er spot holdbar i 24 timer.
· Matrix: HCCA (α-Cyano-4-hydroxycinnamic acid). Krystalliserer prøvemateriale. Uløst Matrix oppbevares på kjølerom B024.
Tillaging av Matrix:
1. Hent 3 Matrix-rør fra kjølerom.
2. Sjekk LOT-nummer. Dersom nytt LOT må dette registreres inn på instrument-PC. Gi beskjed til superbruker.
3. Tilsett 250 µL OS til hvert rør.
4. Vortex minimum 5 minutter. Sjekk at alt materiale er løst opp i bunnen. Kakk løsningen ned mot benken slik at det ikke blir liggende rester i lokket.
5. Skriv dato på lokket.
70 % maursyre (FA): Benyttes til eDT-prosedyrer og ekstraksjon. Utføres i avtrekk med hansker. Oppbevares i avtrekk. Ny bruksløsning lages ukentlig.
Tillaging av 70 % maursyre
1. Tilsett 300 µL HPLC-gradert vann i eppendorf-rør med skrukork.
2. Tilsett 700 µL ren maursyre.
3. Vortex godt.
Analyseutstyr og klargjøring av disse
MBT FAST Shuttle: Kan benyttes i alle arbeidsprosesser for å forkorte tørketiden og bedre krystalliseringsevnen til Matrix. Når påskrudd vil varmeblokken varmes opp til 35°C. Skrus automatisk av etter 30 minutter. OBS! Benyttes kun for engangsplater ved kjøring på Sirius.
Engangsplater: Kan benyttes i alle arbeidsprosesser.
Flerbruksplater: Kan benyttes i alle arbeidsprosesser med unntak av muggsopp.
Rengjøring av flerbruksplater
Utføres i avtrekk med vask. Husk å skru på vifte og sjekk at spjeld er åpent.
1. Legg plater som skal rengjøres i en glassbeholder med linsepapir i bunn.
2. Dekk med benksprit (70 %) og la stå i 5 minutter
3. Skyll platene godt under springvann.
4. Benytt linsepapir dekt i benkesprit til å rengjøre spottene på platene.
5. Skyll platene godt under springvann og tørk av med linsepapir.
6. Legg platene tilbake i glassbeholderen. Avsett 100 µL ± 10 µL 80% TFA og rengjør alle spotter med en vattpinne.
7. Skyll platene godt med HPLC-gradert vann. Tørk godt av med linsepapir og la platene lufttørke i 15 minutter ved romtemperatur.
Feilkilder og begrensninger
· Sepsityper:
Hvis lyseringsbuffer inneholder presipitater, oppbevar kit i minst 1 time ved 20-25 grader og vortex røret før åpning. Dersom presipitatene ikke forsvinner, må kittet forkastes. Ta kontakt med faggruppen.
· Mixed culture hints på sepsityper:
Kan gi falske resultater. Vi hensyntar ikke beskjed om polymikrobielle funn. Eventuelle hint må bekreftes med oppsett fra vekst.
· Tvetydige resultat (Konsistenskategori B): Resultater hvor flere ulike mikrober gir høy konfidens identifikasjon. Største feilkilder ligger i det preanalytiske (ikke renspredd isolat eller krysskontaminasjon i prøvepreparering).
· Dyrkningsforhold:
Streptococcus pneumoniae: Kultur bør ikke være eldre enn 24 timer for å unngå autolyse.
Nocardia: Kultur bør ikke være eldre enn 48 timer.
Sopp: Kultur bør være mellom 18-48 timer og inkubert ved 29°C ± 2°C
· Ingen identifikasjon ved oppsett
Kan blant annet skyldes forurenset matrix, uren plate eller for lite eller for mye prøvemateriale på spot.
Bilde 1.0: Ideelt utstryk på bioplate er demonstrert i rad B. Rad A er tilsatt for mye og rad C for lite.


· Se egne begrensinger knyttet til identifikasjon under «Vurdering av svar»
Fremgangsmåte/Utførelse av analysen
Generelle Merknader
· Benytt FAST-shuttle for å få bedre krystallisering av Matrix. Dersom dette ikke er mulig skal spot tørkes i romtemperatur, ikke i varmeskap.
· Det må utføres en BTS-kalibrering ved hver kjøring. Ved 1. oppsett hver morgen tas frysrør opp fra fryser. Dette vil være nok til ca. 6 kjøringer gjennom en arbeidsdag. Skriv dato på røret og plasser i stativ på benk. Det settes opp fortrinnsvis 2-3 før lunsj, og 3-4 etter lunsj, men dette kan vurderes etter behov.
· TIPS. Dersom man har renspredd flere uidentifiserte isolat på samme prøve og man mistenker at man har flere renspredninger av samme isolat kan disse med fordel kjøres "offline" ved å merke prøver i arbeidsark med bokstaver foran instrumentnummer (f.eks. isolat a-f), og så tildele disse isoaltnummer etter kjøring.
· For identifikasjon av gjærsopp anbefales to spot per agens. DT kan fungere, men celleveggen krever ofte eDT eller ekstraksjon for bedre spekter. (5)
· For identifikasjon av grampositive anaerobe bakterier anbefales eDT. (6)
· Ved mistanke om Bacillus anthracis enten i blodkulturflaske (spore-dannende, store og rette grampositive staver som er ubevegelige i våtpreparat) eller isolat i vekst (Bacillus uten hemolyse) samt kliniske opplysninger som vekker mistanke: Se ALM-MM-Id; Identifisering av Bacillus spp
Forordning Av Prøver På Epicenter
Velg ikonet for malditof i verktøylinjen: ![]()
Scann platenummer inn i epicenter, eventuelt velg nummer på flebruksplate i rullegardinmeny.
Det må alltid være med en posisjon med BTS på hvert oppsett. Velg ledig posisjon på platen og scann prøver fortløpende. Husk å velg riktig isolatnummer. Dette er avgjørende for å få riktig overføring til Beaker. Ved oppsett av paralleller er det viktig å sette punktum før eller etter instrumentnummer for å unngå duplikater i epicenter.
For sepsityper, registrer preparatetiketten slik at det enkelt kan spores tilbake ved behov.
Prøvepreparering
OBS! Les kapittelet HMS/Sikkerhetsinformasjon.
Velg riktig fremgangsmåte etter funn/prøvemateriale.
Protokoll for modul biotyper og sepsityper
· Direct Transfer (DT): Førstehåndsvalget ved alle oppsett, hvor man setter opp spot + Matrix. Unntak: Fæcesisolat og muggsoppisolat.
· Extended Direct Transfer (eDT): Direkte oppsett med maursyre. Andrehåndsvalget dersom DT ikke fungerer, eventuelt førstehåndsvalg for gjærsopp og anaerobe bakterier.
· Ekstraksjon (EXT): Dersom det ikke oppnås tilfredsstillende resultat med DT eller eDT utføres full ekstraksjon.
Protokoll for modul filamentous fungi (muggsopp og dermatofytter)
· Mycelium Transfer (MyT): Direkte oppsett med maursyre.
· EXT: Dersom det ikke oppnås tilfredsstillende resultat med MyT utføres full ekstraksjon. Inkubasjonstid påvirker resultat av Maldi-TOF analyse. Generelt er det anbefalt å plukke fra unge kolonier, ofte 48-72 timers dyrkningstid, men også ned i 24 timer har vist å gi gode resultat. Ved manglende identifikasjon eller lav score kan nytt forsøk fra kultur som har vært dyrket videre i 1-2 dager være nyttig (8).
Dersom BTS kalibrering er OK vil instrumentet fortsette med prøvene. Dersom kalibrering feiler så vil kjøringen avbrytes. Kjøringen kan restartes, eventuelt legg til en ny spot BTS til oppsettet.
Utførelse
Tabell 1.1: Fremgangsmåte Biotyper DT
|
FREMGANGSMÅTE BIOTYPER DT (Direct transfer)
OPPSETT UTFØRES PÅ BENK |
|
1. Bruk en tannpirker og
avsett litt materiale fra en enkeltliggende koloni på spot. Forsøk å få et
jevnt, tynt lag for best mulig resultat. Bytt tannpirker for hver spot. For
raskere tørking av BTS kan FAST-shuttle benyttes. |
Tabell 1.2: Fremgangsmåte Biotyper eDT
|
FREMGANGSMÅTE BIOTYPER eDT (Extended Direct Transfer) |
|
1. Bruk en tannpirker og
avsett litt materiale fra en enkeltliggende koloni på spot. Forsøk å få et
jevnt, tynt lag for best mulig resultat. Bytt tannpirker for hver spot. For
raskere tørking av BTS kan FAST-shuttle benyttes. |
Tabell 1.3: Fremgangsmåte Biotyper EXT
|
FREMGANGSMÅTE BIOTYPER EXT (Ekstraksjon) |
|
1. Pipetter 300 µl
HPLC-gradert vann i et eppendorfrør. |
Tabell 2.1: Fremgangsmåte Sepsityper DT og eDT
|
FREMGANGSMÅTE SEPSITYPER DT og eDT VIDERE ARBEID UTFØRES I AVTREKK VED FÆCESPLASSEN |
|
1. Benytt nål til å
overføre 1 mL blod fra blodkulturflaske til et eppendorfrør. PUNKT 1 UTFØRES I AVTREKK PÅ PRØVEPLASS, VIDERE
ARBEID FRA PUNKT 2-8 UTFØRES I AVTREKK VED FÆCESPLASS.
|
Tabell 2.2: Fremgangsmåte Sepsityper EXT
|
FREMGANGSMÅTE SEPSITYPER EXT (Ekstraksjon) |
|
Benytt pellet fra DT-prosedyre (holdbar 1 time).
1. Pipetter 300 µl
HPLC-grad vann i eppendorfrør med sepsityper pellet og resuspender med
pipette. |
Tabell 3.1: Fremgangsmåte Filamentøse sopp MyT
|
FREMGANGSMÅTE FILAMENTØSE SOPP MyT (Mycelium Transfer) |
|
1. Pipetter 1 µL 70 % maursyre
til tildelt spot. |
Tabell 3.2: Fremgangsmåte Filamentøse sopp EXT
|
FREMGANGSMÅTE FILAMENTØSE SOPP EXT (Ekstraksjon) OPPSETT UTFØRES I AVTREKK VED FÆCESPLASS MED SMITTEFRAKK OG NITRILHANSKER OBS! Må kun utføres på engangsplater |
|
1. Pipetter 300 µl
HPLC-grad vann i et eppendorfrør. |
Forordning Av Prøver På Instrument-Pc
Logg inn på MBT Compass HT IVD
Brukernavn ved daglig drift: tof-user
Brukernavn for superbrukere: lab-manager
Passord: bruker
Bilde 2.0: Oversikt over funksjoner i MBT Compass
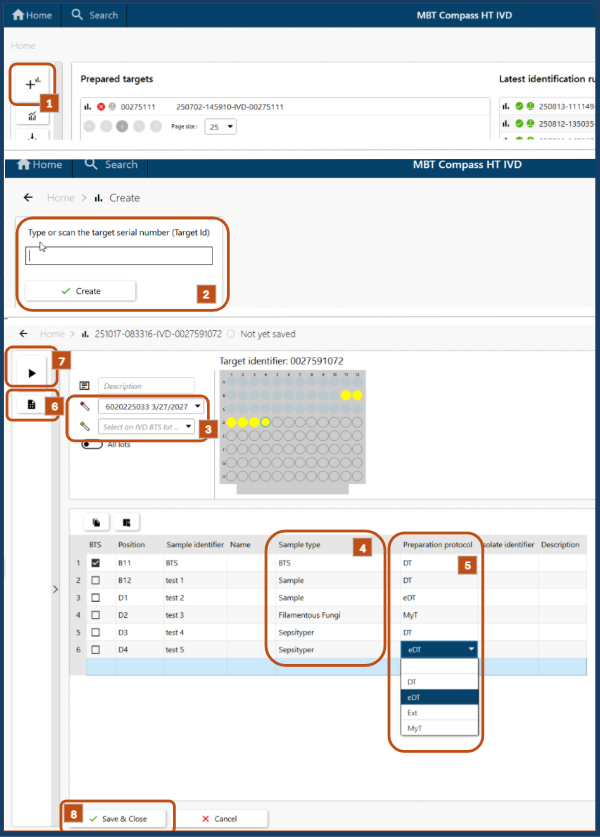
1. Trykk på plussymbolet i hovedbildet på MBT Compass HT IVD
2. Scann platens barkode
3. LOT på siste registrerte Matrix kommer automatisk opp. I feltet under velges aktuell BTS LOT.
4. Posisjonen til BTS lagt inn på epicenter må manuelt endres til sample type «BTS». For resterende prøver velges aktuell modul:
- Sample vil gjelde alle normale oppsett
- Filamentous Fungi velges for muggsoppisolat
- Sepsityper velges for oppsett direkte fra blodkultur.
5. Under preperation protocol velges fremgangsmåte:
- DT = Direct Transfer
- eDT = extended Direct Transfer (maursyre)
- Ext = Extraction
- MyT = standard oppsett for muggsopp med maursyre
6. Ved behov kan arbeidsark printes ut, men dette kan også gjøres via epicenter. Aktuelt for oppsett i avtrekk.
7. Start kjøring når platen er satt inn i instrumentet.
8. Ved behov for å utsette kjøring kan oppsett lagres og hentes inn igjen senere.
Vurdering av svar
Det må alltid gjøres en helhetlig vurdering av svarets pålitelighet. Konsistenskategori skal være A for at man uten videre skal kunne godta en identifikasjon. For biotyper gjelder >2.0 (og konsistenskategori A) for sikker identifikasjon til species nivå og >1.8 til genus nivå. For Filamentous fungi og Sepsityper gjelder >1,8 (og konsistenskategori A) for sikker identifikasjon til species nivå og >1,6 til genus nivå.
Alle identifikasjoner med ID score 1,70 - 1.99: Vurder besvaring av identifikasjon på kun genusnivå i hvert tilfelle (f.eks. Corynebacterium sp.). Isolat fra blodkultur og spinalvæske skal aldri besvares på kun genusnivå. For andre sterile materialer bør lege konfereres. Dersom minst fire av de først foreslåtte identifikasjoner på en spot viser samme species, forsterkes sannsynligheten for korrekt artsidentifikasjon.
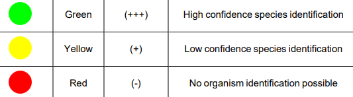
Log Score Og Matching Hints
Tabell 4.1: Beregning av Log Score
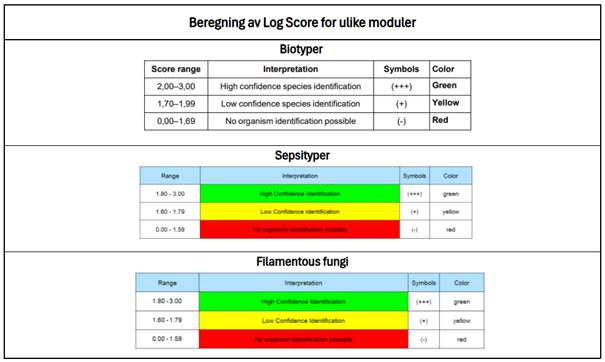
Spesielle bemerkninger for gjærsopp:
Bruker anbefaler cut-off for artsidentifikasjon log score >2.0, men flere publikasjoner beskriver sikker identifikasjon av gjærsopp til artsnivå med log score >1.7 i Brukerdatabasen, forutsatt forøvrig entydige identifikasjon/ «consistency» og paralleller- på lik linje med kriterier for bakterieartsidentifikasjon. (5)
Tabell 4.2: Ulike faktorer som påvirker kvaliteten av et resultat
|
Forklaring på faktorer som påvirker påliteligheten til et resultat. |
||
|
Log Score |
Biostatisk parameter som reflekterer påliteligheten til en identifikasjon basert på likheten mellom et referansespekter og et prøvespekter. Påliteligheten øker jo høyere denne verdien er. |
|
|
Log Score indicator |
Fargeangivelse som angir konfidensnivået til en identifikasjon gjennom farger som reflekterer Log Score-verdi og plussymboler som reflekterer konfide
nsverdi: |
|
|
Best Match |
Organismen med høyeste Log Score |
|
|
Second Best Match |
Organismen med nest høyeste Log Score |
|
|
Consistency |
Benytter de to beste MSP (Main Spectrum) matcher (Best og Second best match) i en kjøring for å beregne en konsistenskategori |
|
|
Matching Hints |
Kommentarer som følger visse identifikasjoner. Den omtaler metodebegrensinger. |
|
|
Konsistenskategorier |
A (Høy konsistens): |
Beste match er en høy konfidens identifikasjon (grønn), mens den
nest beste match har: |
|
B (Lav konsistens): |
Beste match har høy konfidens (grønn) eller lav konfidens (gul),
mens den nest beste match har: |
|
|
C (Ingen konsistens) |
Kravene for høy eller lav konsistens er ikke møtt. F.eks. Forskjellige genusnivå |
|
|
Eksempler på forskjellige konsistenskategorier |
||
|
Beste match |
Nest beste match |
Konsistenskategori |
|
E.coli (Høy konfidens Genus A, species A) |
E.coli (høy konfidens Genus A, species A) |
A |
|
E.coli (Høy konfidens Genus A, species A) |
E.scherichia fergusonii (Høy konfidens Genus A, species B) |
B |
|
E.coli (Høy konfidens Genus A, species A) |
E.scherichia fergusonii (Lav konfidens Genus A, species B) |
A |
|
E.coli (Lav konfidens Genus A, species A) |
E.scherichia fergusonii (Lav konfidens Genus A, species B) |
B |
|
E.coli (Høy konfidens Genus A, species A) |
Gardnerella vaginalis (Høy konfidens Genus B, species B) |
C |
|
E.coli (Høy konfidens Genus A, species A) |
Gardnerella vaginalis (Lav konfidens Genus B, species B) |
C |
|
E.coli (Høy konfidens Genus A, species A) |
No ID |
A |
|
E.coli (Lav konfidens Genus A, species A) |
No ID |
B |
Særlige Bemerkninger Knyttet Til Utgivelse Av Funn Og «Matching Hints»
Man skal alltid hensynta «Matching Hints» dersom dette forekommer. Disse gir verdifull informasjon om metodebegrensinger knyttet til korrekt speciesidentifikasjon, som f.eks. pneumokokker, eller genusidentifikasjon som f.eks. E.coli og Shigella. Dette gjelder både mikrober som er vanskelig å skille, samt mikrober som skal svares ut som del av komplekser eller grupper. Se relatert lenke «Matching Hints» under relatert for hvordan disse skal besvares.
Dersom isolat er identifisert etter ny nomenklatur eller omtales under flere navn gir vi ut nytt navn (dersom det er bygd i beaker) og inkluderer nytt/gammelt navn i kommentarfelt. F.eks. «Winkia neuii tidligere kjent som Actinomyces neuii».
Besvarelse av E.coli:
Differensering mellom E. coli, diarefremkallende E. coli og Shigella spp. hos stammer isolert fra fokus utenfor GI-traktus er nødvendig for blodkultur og sterile materialer, samt når det er klinisk mistanke om at stammen har sammenheng med gastrointestinal infeksjon. I slike tilfeller vurderes laktosespalting på MacConkey . Dersom isolatet ikke gir rosa kolonier på MacConkey skal det spres til SS/XLD-agar for å utelukke funn av Shigella. For resultater fra sepsityper må identifikasjon kun rapporteres dersom det ikke foreligger klinikk som gir mistanke om Shigella.
For vurdering av SS/XLD-agar, se ALM-MM-Fæces; Shigella dyrkning
Se ellers aktuelle prosedyrer:
ALM.MM-Fæces; Vurdering og besvaring av funn (Ikke tilgjengelig)
ALM-MM-Fæces; Vurdering, innlapping og primærutsæd av fæcesprøver
Besvarelse av Neisseria meningitidis
Identifikasjon av N. meningitidis kan aksepteres etter
produsents kriterier som foreløpig identifikasjon, særlig ved alvorlig klinikk
og/eller isolat fra sterilt område (f.eks. blod og cerebrospinalvæske). Vurder
16S rRNA eller målrettet PCR ved behov for rask avklaring.
For blodkultur og spinalvæske gir vi ut med sannsynlig Neisseria
meningitidis, men med kommentar om at stammen er sendt SOH. For annet
prøvemateriale gis ut Neisseria spp. og at stammen er sendt SOH.
Ved funn i genitalia vurder mulighet for uretrittassosiert N. meningitidis. Suppler med molekylær testing (16S PCR). (9)
Besvarelse av Streptococcus pneumoniae
Ved identifikasjon som S. mitis, S.oralis, S. pneumoniae eller S. pseudopneumoniae kan disse besvares som S. pneumoniae dersom optochintest, dryspot og/eller morfologi underbygger dette. Eventuell supplering med galletest kan benyttes ved tvil.
Foreløpig besvarelse av S.dysgalacticae på Sepsityper
Før vi har vekst til å utføre agglutinasjonstest, besvares S.dysgalacticae med koden .SDYS («Nærmere identifikasjon og følsomhetsbestemmelse ventes ferdig i morgen. Kan gi samme type infeksjoner som gruppe A streptokokker.»)
Besvarelse av muggsopp
Ved god score skal besvarelse av muggsopp inneholde speciesidentifikasjon, samt tilhørende gruppe eller kompleks dersom dette er oppgitt i «Matching hints».
Med tanke på hva som er bygget i beaker, må man ved noen rapporteringer endre litt på hva som legges i isolatfelt og hva som legges som kommentar. Utgangspunktet er at speciesidentifikasjon legges i isolatfelt, og tilhørende gruppe/kompleks legges i kommentarfelt.
Eks:
«Vekst av Aspergillus tamarii»
«Tilhører Aspergillus flavus komplekset»
Tabell under viser en oversikt over Aspergillus inkludert i databasen. Konferer faggruppe eller medisinsk faglig rådgiver dersom man har funn som ikke er omtalt i tabellen og som har «matching hints».
Tabell 5.0: Besvarelse av Aspergillus sp.
|
Besvarelse av Aspergillus species |
|||
|
Begrensninger i databasen (Species som ikke kan skilles) |
Speciesnavn som rapporteres |
Kommentar til svaret (det som står i parentes skal ikke ut i svar) |
|
|
A. flavus |
Aspergillus flavus kompleks |
Nærmere bestemt Aspergillus flavus-oryzae gruppen |
(Aspergillus flavi gruppen) |
|
A. oryzae |
|||
|
|
A. parasiticus |
Tilhører Aspergillus flavus kompleks |
|
|
A. tamarii |
|||
|
A. fumigatus |
Tilhører Aspergillus fumigatus kompleks |
(Aspergillus fumigatus gruppen) |
|
|
A. lentulus |
|||
|
A. nidulans |
Tilhører Aspergillus nidulans kompleks |
(Aspergillus nidulantes gruppen) |
|
|
A. sydowii |
|||
|
A. unguis |
|||
|
A. versicolor |
|||
|
A. brasiliensis |
Tilhører Aspergillus niger kompleks |
(Aspergillus nigri group) |
|
|
A. japonicus |
|||
|
A. niger |
|||
|
A. terreus |
Tilhører Aspergillus terreus kompleks |
||
|
A. calidoustus |
Tilhører Aspergillus usti gruppen |
||
|
A. ustus |
|||
|
A. ochraceus |
Tilhører Aspergillus circumdati gruppen |
||
|
A. sclerotiorum |
|||
|
A. westerdijkiae |
|||
|
A. tritici |
Tilhører Aspergillus candidi gruppen |
||
|
A. ruber |
Tilhører Aspergillus aspergillus gruppen |
||
|
A. montevidensis |
|
||
|
A.clavatus |
|||
|
A. lizukae |
|||
|
A. japonicus |
|||
|
A. penicillioides |
|||
|
A. pseudoglaucus |
|||
|
A. pulvinus |
|||
|
A. tritici |
|||
|
A. candidus |
Aspergillus species (F45 LLH) |
Lar seg ikke nærmere identifisere. |
|
|
A. campestris |
|||
|
A. pragensis |
|||
|
A. subalbidus |
|||
Besvarelse av dermatofytter (f.eks. Trichophyton sp., Microsporum sp., Epidermophyton sp.)
Ved funn av dermatofytter bør morfologi sammenholdes med klinikk, prøvelokalitet, resultat ved massespektrometri og eventuelt også resultat fra supplerende tester før prøven besvares. I de tilfellene der korrekt artsidentifikasjon vurderes som klinisk relevant, enten ved alvorlige og/eller uttaltee infeksjoner, eller ved opplysninger om terapisvikt, bør prøven videresendes referanselab for bekreftelse av ID ned til species-nivå (7). Konferer faggruppe eller medisinsk faglig rådgiver ved funn av dermatofytter.
Besvarelse av gjærsopp med ny taksonomi
Det pågår en endring i gjærsopptaksonomi hvor en rekke Candida spp. har endret navn. I tabell 6.0 er det listet opp ny nomenklatur som Bruker har tatt i bruk, med forslag om besvarelse (10)
Tabell 6.0 Besvarelse av visse Candida sp.
|
ID på MaldiTOF (v. 13) |
Besvaring i Beaker |
Kommentar til funn |
|
Debaryomyces hansenii |
Candida famata |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Debaryomyces hansenii |
|
Meyerozyma guilliermondii |
Candida guilliermondii |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Meyerozyma guilliermondii |
|
Pichia cactophila |
Candida inconspicua |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Pichia cactophila |
|
Kluyveromyces marxianus |
Candida kefyr |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Kluyveromyces marxianus |
|
Pichia kudriavzevii |
Candida krusei |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Pichia kudriavzevii |
|
Pichia fermentans |
Candida lambica |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Pichia fermentans |
|
Clavispora lusitaniae |
Candida lusitaniae |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Clavispora lusitaniae |
|
Wickerhamiella pararugosa |
Candida pararugosa |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Wickerhamiella pararugosa |
|
Cyberlindnera jadinii |
Candida utilis |
Nomenklatur av gjærsopp er under revisjon, nytt foreslått navn: Cyberlindnera jadinii |
Svarrapportering
Overføring skjer automatisk til Beaker etter endt kjøring. Kun svar med konsistenskategori A vil overføres. Dersom resultat legges inn manuelt etterrekvireres malditof som egen komponent. For å sikre sporing legges score i kommentarfelt under komponent.
Vedlikehold
Detector Check
Monitorering av detektorens ytelse. Gir mulighet til å kompensere for slitasje ved å regulere spenning (volt).
Operasjonen tar 5 minutter og bør utføres månedlig. På Sirius vil man få automatisk varsel om når det er behov for detektorsjekk, før en kjøring. Hak av ja på dette, så vil test gjennomføres og spenning justeres automatisk etter rutinekjøring.
Source Cleaning
Utføres rutinemessig ukentlig. Se eget vedlikeholdsskjema på teams.
Logg på flexControl (MBT Compass må lukkes først).
Under fanen «Status» velges «Details» og «Start Cleaning». Prosedyren tar ca. 30 minutter.
Bilde 3.0 Oversikt flex-control.
![]()
![]()
![]()
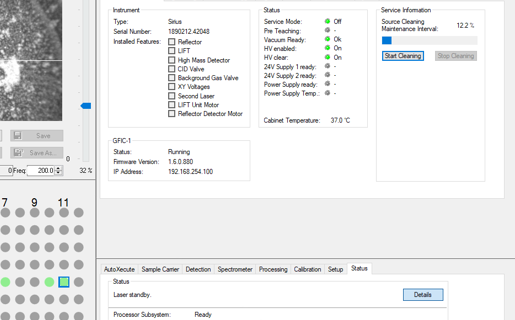
OBS! Under denne operasjonen vil instrumentet kjøre kammeret i ut-posisjon for å frigjøre IR-laseren. Ikke åpne luken så lenge source clean pågår!
Feilsøking
Dersom LED-indikator på fremsiden av instrumentet lyser rødt indikerer dette en feil.
Lukk MBT Compass og åpne FlexControl. Error-meldinger legger seg på bunnlinjen her.
Sjekk om det er noe galt med vakuumet. Gå til status og detaljer. Velg vakuumfanen og “Gauges”. Dersom det er et rødt lys knyttet til «Source High» er det noe galt med vakuumet. Kjør plate ut og sjekk O-ringen og kammeret for partikler. Benytt finger for å rengjøre O-ringen (OBS! Ikke benytt alkohol eller andre desinfeksjonsmidler som kan skade O-ringen). Fjern eventuelt støv i kammeret med q-tips og vann.
Ved behov for fullstending «Shutdown» er det viktig å stenge ned all software og PC. Av/på-knapp finnes på baksiden av instrumentet. Vent 30-60 sekunder før instrumentet skrus på igjen. Vent til LED lyser grønt før PC slås på igjen.
Kontakt support dersom dette ikke hjelper:
Mail:
support.bdal.nordic@bruker.com
Inkluder følgende:
· Instrumentets serienummer: 189021242048
· Instrument statusrapport (Zip fil kan lages i MBT Compass under «Maintenance», «Trouble shooting» og “Create status report”.
· Beskrivelse av feil
Telefon
+46 8655 2520
Oppgi serienummer: 189021242048
Ta kontakt med medisinsk teknisk avdeling for oppkobling av VPN ved behov for fjernstyring (Remote support)